Verschaffen Sie sich einen Überblick über die drei größten Herausforderungen bei der Infektionskontrolle und der Aufbereitung. Erfahren Sie außerdem, wie sterile Einweg-Endoskope Zeit sparen, die sonst für die Aufbereitung verwendet wird. Zudem reduzieren sie das Risiko einer Kreuzkontamination und verbessern die Patientensicherheit.
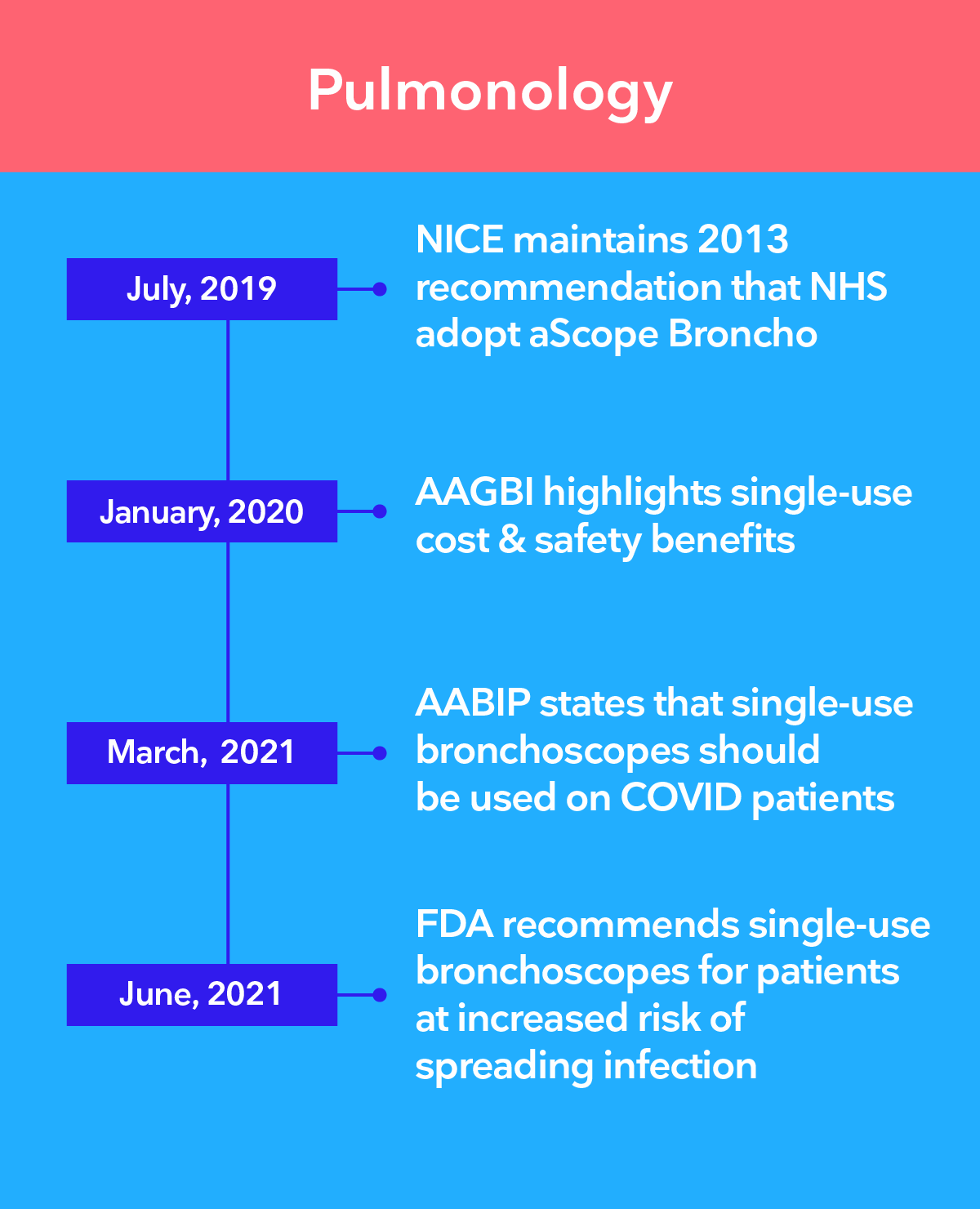
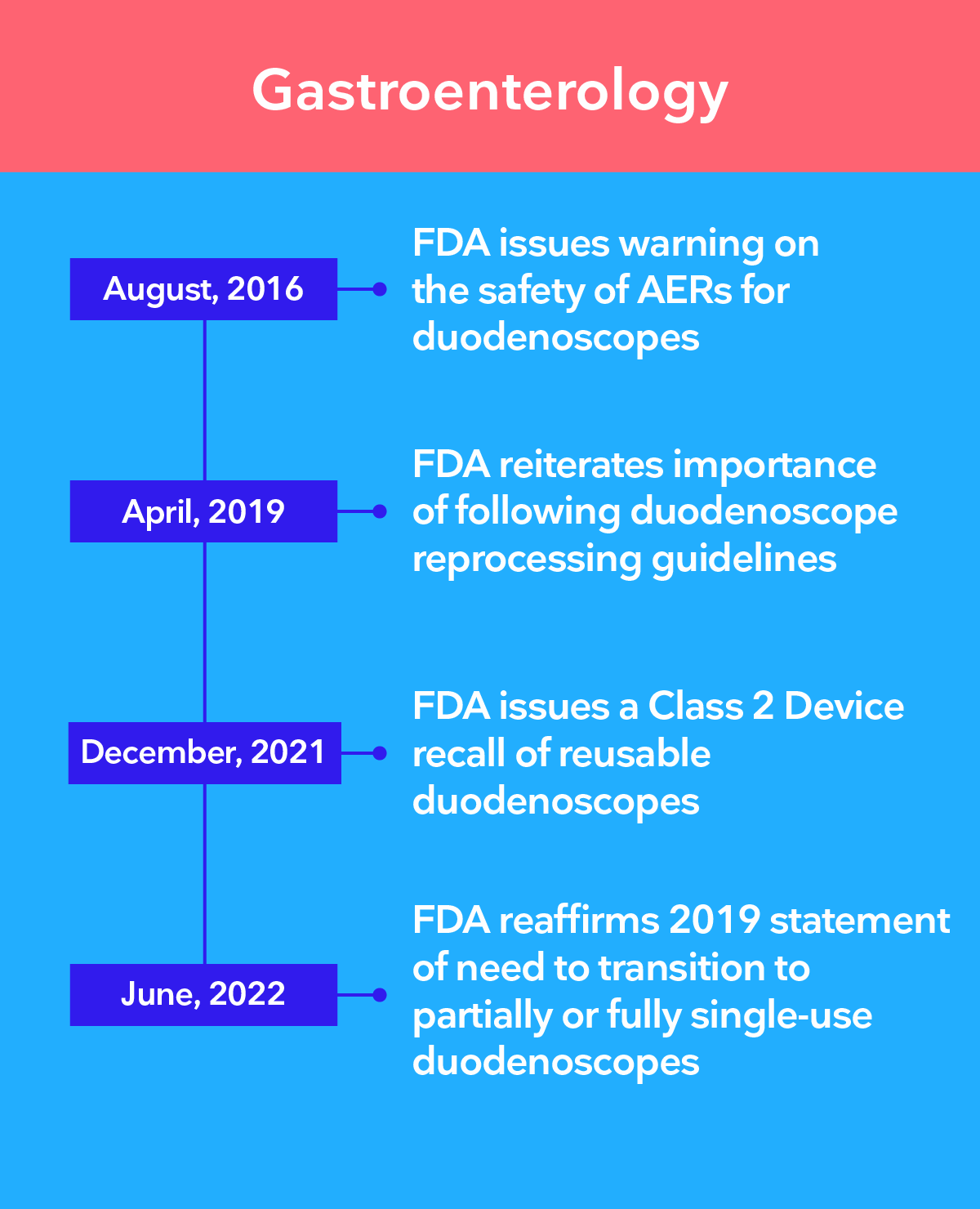
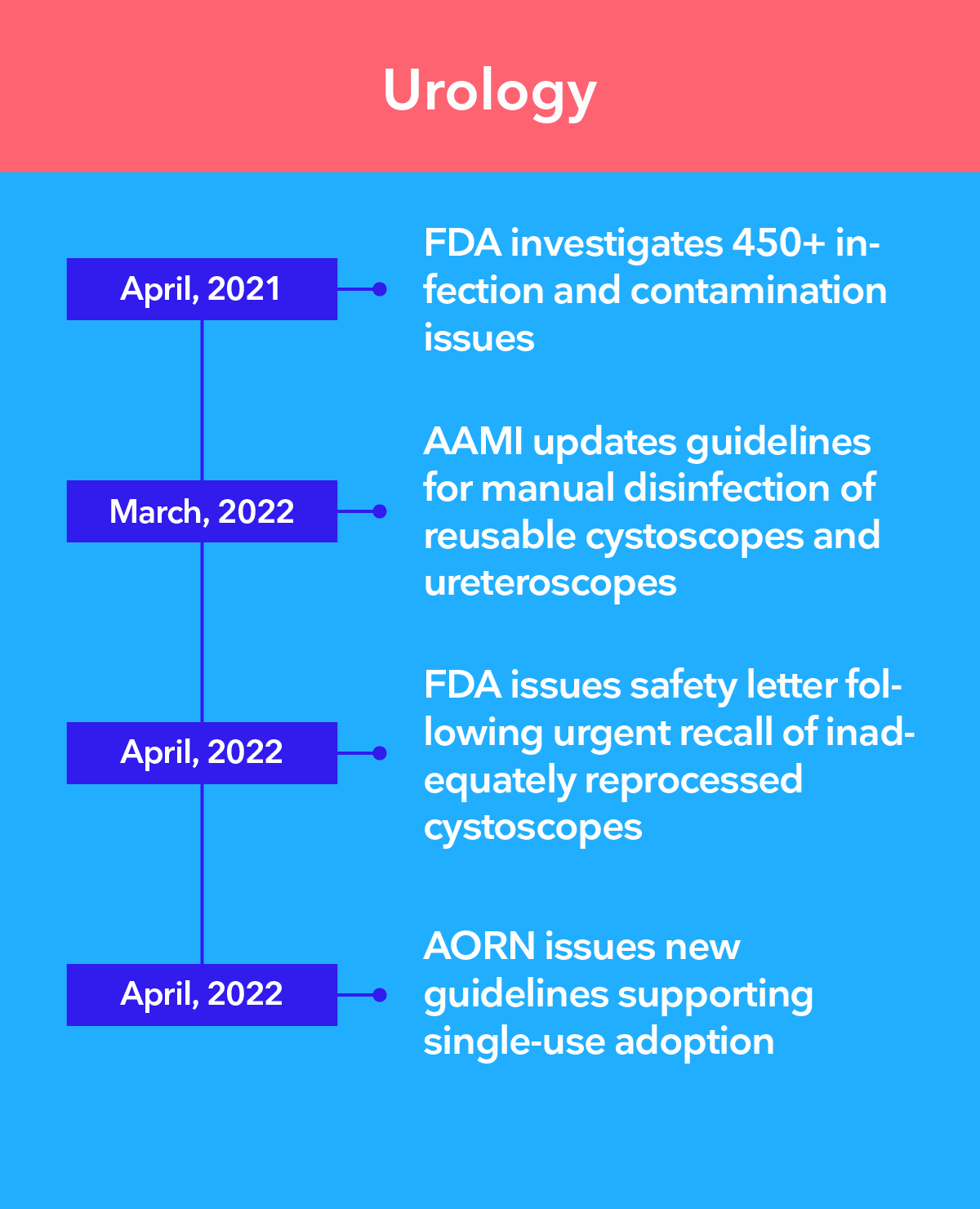
Führende Behörden empfehlen die Umstellung auf Einweg-Endoskope
Die Bedenken wachsen, dass selbst bei den strengsten Desinfektionsverfahren nicht gewährleistet werden kann, dass Mehrweg-Endoskope steril sind. Ambu® Einweg-Endoskope eliminieren das Risiko einer Kreuzkontamination, da sie stets steril zum Einsatz kommen.
Wenn der Sicherheitsspielraum für die Aufbereitung von Einweg-Endoskopen so klein ist, dass die perfekte Einhaltung von mehr als 100 Seiten Gebrauchsanweisung des Herstellers nötig ist, dann ist das Design zu komplex, die mikrobielle Belastung zu hoch und der Prozess zu fehleranfällig, um in der Praxis durchführbar zu sein.7
William A. Rutala, PhD, MPHX
Die drei größten Herausforderungen bei der Infektionskontrolle in der Endoskopie
Komplexe, kostenaufwändige und letztlich ineffektive Reinigungsprozesse
Mehrere Studien haben gezeigt, dass unabhängig von den eingesetzten Ressourcen und genauer Einhaltung der Richtlinien kein Reinigungsprozess alle Mikroorganismen effektiv entfernt.1-4 Dabei ist es unerheblich, ob die Aufbereitung mit High-Level-Desinfektion (HLD), doppelter HLD oder HLD in Kombination mit Sterilisation durchgeführt wurde.5-6
Die nachstehend aufgeführten Schritte stellen eine verkürzte Version der empfohlenen grundlegenden Aufbereitungsmaßnahmen dar. In der Realität kann es mehr als 100 Arbeitsschritte geben.7
Schritte der Aufbereitung:
VORREINIGUNG
UNVERZICHTBAR FÜR DIE VERMEIDUNG VON BIOFILM
Muss nach der Anwendung zeitnah und sorgfältig gemäß der Gebrauchsanweisung durchgeführt werden.
DICHTIGKEITSTEST
INTERNE/ EXTERNE BESCHÄDIGUNGEN ERKENNEN
Schäden können zu unzureichender Desinfektion und weiterem Verschleiß führen.
MANUELLE REINIGUNG
WICHTIGSTER SCHRITT ZUR DESINFEKTION
Eine sorgfältige Vorreinigung ist Voraussetzung für HLD und Sterilisation.
VISUELLE ÜBERPRÜFUNG
ZUSÄTZLICHE SICHERHEIT
Das komplexe Design flexibler Endoskope erschwert die visuelle Erkennung von Schäden.
DESINFEKTION
ANWEISUNGEN EINHALTEN
Herstellerangaben zu Desinfektionmittelkonzentration und Einwirkzeit sind strikt einzuhalten.
LAGERUNG
GESCHÜTZT VOR FEUCHTIGKEIT
Unsachgemäße Lagerung kann zu Bakterienwachstum führen.
DOKUMENTATION
ENTSCHEIDEND FÜR DIE QUALITÄTSSICHERUNG & RÜCKVERFOLGBARKEIT
Dokumentation der oben genannten Schritte ist bei jeder Aufbereitung eines Endoskops erforderlich.
WIEDERHOLUNG NACH JEDEM EINGRIFF
EIN FORTLAUFENDER PROZESS
Die hier gezeigten Schritte umfassen nur die grundlegenden Maßnahmen. Individuelle Richtlinien sollten in jeder Einrichtung von einem interdisziplinären Team erarbeitet werden.
Endoskope sind grundsätzlich schwer zu reinigen
Lange, schmale Kanäle, schwer zugängliche Stellen1, 8-9 und Abnutzungserscheinungen4-5, 10-11 sowie Rillen, die sich durch den routinemäßigen Gebrauch und die Reinigung bilden, machen Endoskope anfällig für Feuchtigkeit und bakterielle Kontamination.
Bakterien können sich in den Fernbedienungstasten, den Anschlüssen des Griffteils, den Vertiefungen des distalen Endes, dem Biopsieanschluss und dem Arbeitskanal aller Endoskope ansiedeln. Bei GI-Endoskopen können sich Bakterien auch in Ventilen und Rädern des Steuergriffs verstecken, zudem ist die komplexe Konstruktion des Duodenoskop-Hebels besonders schwer zu reinigen.
Tatsächlich hat die ECRI - eine gemeinnützige US-Organisation für Patientensicherheit - das Potenzial für Kreuzkontaminationen und die unzureichende Reinigung von Endoskopen mehrfach in ihre jährliche ECRI-Liste der “Top 10 Health Technology Hazards” aufgenommen.
Orte, an denen sich Erreger gerne verstecken
- Steuerhebel
- Absaugtaste
- Endoskoptasten
- Fernbedienungstasten, Ventile und Abwinkelungsräder
- Biopsieanschluss
- Distales Endoskopende
- Distales Ende mit Hebel
- Arbeitskanal
Die Zunahme multiresistenter Keime
Die Zunahme von multiresistenten Organismen (MDROs), die auch als Superbugs bezeichnet werden, hat die Reinigung von Endoskopen in den letzten Jahren noch herausfordernder gemacht.12-13 Seit 2000 wurden beispielsweise mehr als 15 Ausbrüche im Zusammenhang mit MDROs gemeldet.14
Ambu Einweg-Endoskope werden steril und einsatzbereit geliefert
Mit Ambu Einweg-Endoskopen können Sie:
Die Tatsache, dass alle Ambu Einweg-Endoskope phthalatfrei sind, eine unserer vielen Umweltinitiativen, trägt ebenfalls zur Patientensicherheit bei.
Erfahren Sie mehr über die Vorteile von Einweg-Endoskopen
Erfahren Sie, wie die sterilen Ambu Einweg-Endoskope eine gleichbleibend hohe Qualität und Performance, bieten Arbeitsabläufe optimieren und Ihnen eine bessere Kostentransparenz in verschiedenen klinischen Bereichen ermöglichen.
Erfahren Sie mehr über Ambu Einweg-Endoskope
Literaturangaben
1. Rauwers AW, Voor in ‘t holt AF, Buijs JG, de Groot W, Erler NS, Bruno MJ, Vos MC, Nationwide risk analysis of duodenoscope and linear echoendoscope contamination, Gastrointestinal Endoscopy (2020).
2. Rex DK, Sieber M, Lehman GA, et al. A double-reprocessing high-level disinfection protocol does not eliminate positive cultures from the elevators of duodenoscopes. Endoscopy. 2018;50(6):588-596.
3. Naryzhny I, Silas D, Chi K. Impact of ethylene oxide gas sterilization of duodenoscopes after a carbapenem-resistant Enterobacteriaceae outbreak. Gastrointestinal Endoscopy (2016).
4. Seidelman JL, Akinboyo IC, Taylor B, Henshaw NG, Abdelgadir A, Gray GC, Smith BA, Lewis SS. Pseudo-outbreak of adenovirus in bronchoscopy suite. Infect Control Hosp Epidemiol. 2021 Aug;42(8):1016-1017.
5. Snyder GM, Wright SB, Smithey A, et al. Randomized Comparison of 3 High-Level Disinfection and Sterilization Procedures for Duodenoscopes. Gastroenterology. 2017;153(4):1018-1025.
6. Ofstead Cori L, Quick Mariah R, Eiland John E, et al., 2017: A glimpse at the true cost of reprocessing endoscopes: Results of a pilot project. www.iahcsmm.org. https://www.bostonscientific.com/content/dam/bostonscientific/uro-wh/portfolio-group/LithoVue/pdfs/Sterilization-Resource-Handout.pdf. Accessed May 28, 2023.
7. Kovaleva J. Infectious complications in gastrointestinal endoscopy and their prevention. Best Pract Res Clin Gastroenterol. 2016;30(5):689-704.
8. Rutala WA, Kanamori H, Sickbert-Bennett EE, Weber DJ. What’s new in reprocessing endoscopes: Are we going to ensure “the needs of the patient come first” by shifting from disinfection to sterilization? Am J Infect Control. 2019 Jun;47S:A62–6.
9. Mark J, Underberg K, Kramer R, Results of duodenoscope culture and quarantine after manufacturer-recommended cleaning process, Gastrointestinal Endoscopy (2020).
9. Gavalda L, Olmo Ana Rosa, Hernandez R, etal., Hospital Bronchoscopy Quality Improvement Group. Respiratory Medicine (2015) 109, 1079-1085.
10. Ofstead CL, Wetzler HP, Heymann OL, Johnson EA, Eiland JE, Shaw MJ. Longitudinal assessment of reprocessing effectiveness for colonoscopes and gastroscopes: Results of visual inspections, biochemical markers, and microbial cultures. Am J Infect Control. 2017;45(2):e26-e33.
11. Barakat MT, Girotra M, Huang RJ, Banerjee S. Scoping the scope: endoscopic evaluation of endoscope working channels with a new high-resolution inspection endoscope (with video). Gastrointest Endosc. 2018;88(4):601-611.e1.
12. Mehta AC, Muscarella LF. Bronchoscope-Related "Superbug" Infections. Chest. 2020 Feb;157(2):454-469
13. US. Food and Drug Administration. Flexible Bronchoscopes and Updated Recommendations for Reprocessing: FDA Safety Communication. FDA Web site. https://www.fda.gov/medical-devices/safety-communications/flexible-bronchoscopes-and-updated-recommendations-reprocessing-fda-safety-communication. Published 2021. Accessed May 28, 2023.
14. Rubin ZA, Kim S, Thaker AM, Muthusamy VR. Safely reprocessing duodenoscopes: current evidence and future directions. Lancet Gastroenterol Hepatol. 2018;3(7):499-508.










